2012年12月号にイナビルは肺炎や入院を防ぐどころか、発熱期間も短縮できないことを報告しました。それを確認するかのように、今年8月のメディカルトリビューン紙に、イナビルの世界展開のための試験を実施していたアメリカのBiota社が、イナビルがインフルエンザ症状に効果がなかったこと、今後の開発を断念したとの記事が載りました。
ご承知の通り、今年4月トーマス・ジェファーソン氏や浜六郎氏などが実施した完璧なコクランレビューは、タミフルとリレンザが合併症や入院を防ぐことはできないとの結論を出しました。これは世界的なニュースとなり、日本でも共同通信社が詳しい情報を配信しました。この後では、タミフルやリレンザを超える効果がなければ海外では売れません。
表1
| 試 験 | 対 象 | 主要評価項目 | 副次評価項目 |
|---|---|---|---|
| J204 日本人 | 小 児 (15才以下) | インフルエンザ罹病時間 (体温の基準:36.9度以下) | (回復するまでの時間等も 併せて検討された) |
| J201 国 内 | 成 人 | 体温が平熱(36.9度以下)に 回復するまでの時間 | |
| A202 台 湾 | 成 人 | 体温が平熱(37.2度以下)に 回復するまでの時間 | インフルエンザ罹病時間 |
| J203 国 内 | 成 人 | インフルエンザ罹病時間 | |
| J301 国 際 | 成 人 | インフルエンザ罹病時間 | |
| J302 日本人 | 小 児 (9才以下) | インフルエンザ罹病時間 | |
| J303 日本人 | 未成年者 (10才代) | インフルエンザ罹病時間 |
イナビルの承認審査用のデータでは、表1の上から3番目、台湾でのプラセボ(偽薬)と比べた臨床試験までは、発熱期間が主要評価項目(アウトカム)でした。ところがこの試験では発熱期間を短縮できないことがわかりました。すると、それ以後はすべて主要評価項目が、表の下の定義の様な「インフルエンザ罹患時間」に変更されました。この定義は、例えば疲労感や鼻症状は治癒の境界があいまいで、かつ「全ての症状が『なし』又は『軽度』に改善し」など極めてあいまいです。これは、医問研が中心になって批判してきた「全般改善度」という主観的・非科学的評価項目に似ています。この日本的非科学的な評価項目が効果のないイナビルを4280円(大人)もする抗インフルエンザ薬として登場させたのです。
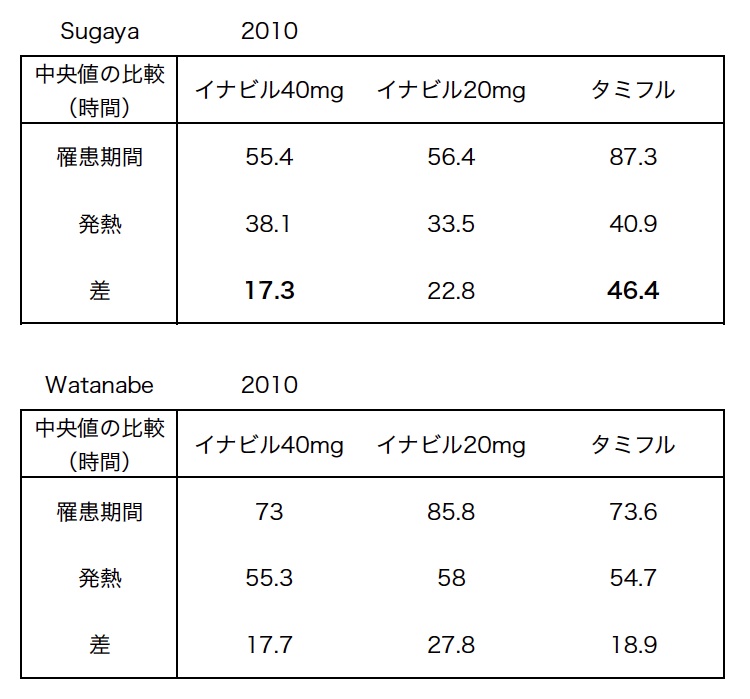
PubMed検索をしてみますと、一応ランダム化比較試験RCTの英語論文も出ているのですが、日本での治験ばかりで、定義は多少違いますが「インフルエンザ罹患時間」を主要評価項目にしています。Pediatricsという権威ある雑誌の論文(Katsumi2012)では、さすがに発熱期間が主要評価項目でした。しかし、これは発熱短縮期間がたった0.6日間のリザベンと比較しで、差がなかったというものです。タミフルと比較した試験(Sugaya2010)では主評価項目は「インフルエンザ罹患期間」で、副次評価項目を発熱にしています。(表2上)この実験では、罹患期間と熱が下がるまでの期間の差がイナビルでは17.3時間ですが、タミフルではなんと46.4時間と極端に違い、とても不自然です。「症状」の期間の差をつけるためにタミフルの罹患期間が操作された可能性も否定できません。ちなみに、Watanabe2010年の実験ではそれはほぼ同じです。(表2下)
今回、Biota社の実験が実施されましたが、同社のプレスリリースでは評価項目は「インフルエンザ症状の緩和時間」となっているだけで詳しくはわかりません。その「緩和期間」は、イナビル40mg群は102.3時間、80mg群は103.2時間でプラセボ(偽薬)の104.1時間と全く差がなかった、すなわちタミフル・リレンザを超えるどころか、全く効かなかったわけです。開発費3億3100万ドルを予定したこの実験が中止されたので、今後の海外での開発は困難と見られています。
日本独自の非科学的な評価項目で無理やり承認させたイナビルも、オノンなど多くの日本だけの薬と同様、科学的根拠のない日本独自の薬になりそうです。効果がない単なる「化学物質」に一回のインフルエンザ罹患で4000円以上保険から支払われるのです。
こんな詐欺的な「薬」は少なくとも保険収載から抹消されるべきです。
はやし小児科 林