紙媒体では2P右下の表の数字が間違っていましたので、訂正をお願いします。
報告は、1)メルクの経口抗コロナ「薬」モルヌピラビルビルは「毒」かも知れない(林)2)浜六郎氏からモルヌピラビルの第Ⅲ相論文の分析で、RCTと言えない背景因子の差があることなどの報告、3)ワクチンの有害作用の日本の報告とRCTでの報告の差(林)、4)入江氏からはコロナワクチンによる小児の死亡例、3回目接種の「副反応」例、オミクロン株の現状などの報告がありました。今回はそのうちの林の2報告をご紹介します。
報告1,メルクの経口抗コロナ「薬」は「毒」かも知れない。
オミクロン株が激増していますが。対策の基本は、医療拡充ですが、それを削り続ける政府の隠れ蓑がいろいろ出されています。その一つが、世界に「先駆けて」の飲む抗コロナ薬の承認です。昨年12月23日米国食品医薬局(FDA)は、メルク社(日本ではMSD)のモルヌピラビル(商品名、ラゲブリオカプセル)を緊急使用許可、その翌日に厚労省医薬・生活衛生局医薬品審査管理課はその「審査結果報告書」を発表し「特例認可」をしています。これが、基本的データを提示しているはずですので、そのデータでの問題点を指摘します。いずれも海外での臨床試験で、日本での臨床試験ではありません。
<効果は「入院又は死亡」を3割減?>
同じアウトカムを7割減らすとした「カクテル療法」と違い3割減です。飲む薬だから仕方がないかと思われる方も多いと思います。しかし、効果を示したデータに大変な問題が隠れていました。
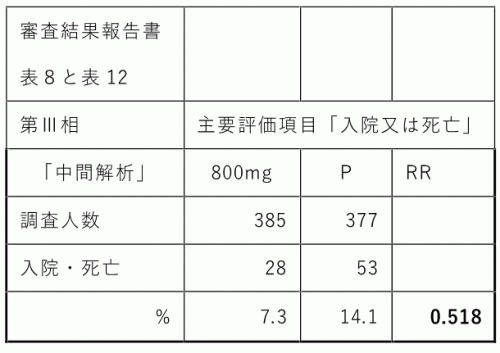
厚労省のデータによれば、まず前半のデータ(中間解析:上表)では、偽薬と比べてリスクを0.518=48.2%減らせたとしています。
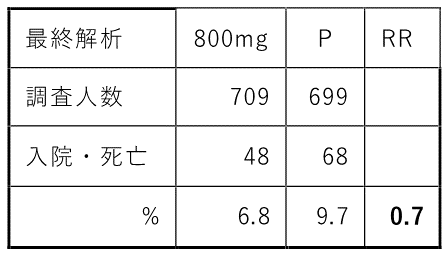
ところが、最終解析(下表)では、RRは0.7で30%しか減らせていません。これが最終的結論になっています。私はこのデータを見て、初めは「効果が薄まったのか?」などとのんきな考えていました。
<中間解析以後は「入院・死亡」が増加>
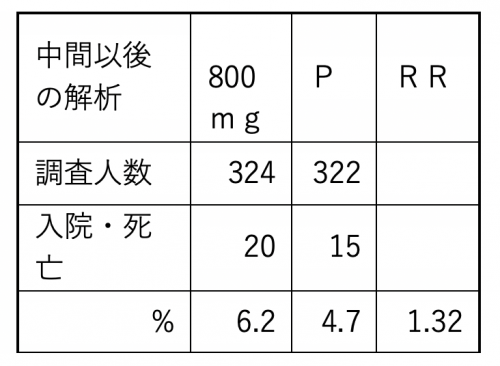
「中間解析後」のデータではどの程度効果を示していたのかを確認するために、「中間解析」のデータと「最終解析」のデータを使って後半のデータを下の表にまとめました。
効果の程度はRRが1.32です。この意味はこの「薬」が、「入院又は死亡」を32%増加させたことを意味します。前半の48%減らせ、後半の32%割増やした結果を合わせると、3割減らしたことになるのです。
前半では4割、後半では3割減らせた、というのならまだわかりますが、後半の試験が病気を悪化させたのですから、大変な問題です。使用する対象によっては「薬」ではなく「毒」となるのです。
さすがに、「審議結果報告」もこれを問題にしていますが、「なお 、無作為化されたすべての被験者の無作為化 29 日目までのデータ の解析結果において、中間解析 結果 と比べて 本薬群とプラセボ群の群間差が小さくなった要因について、申請者により中間解析前後での被験者背景や試験環境の相違等の影響について検討が行われたものの明らかな要因は特定されなかった。」要するに、理由がわからなかった、と記述しているだけです。
「薬」か「毒」かの分かれ目なのに、理由がわからないから、それでいいんじゃないか、というのはあまりにもずさんです。中間解析以後は害になるのですから、それらの解析自体に相当な「操作」がされている可能性があります。全ての元データが公開されるべきです。
<催奇性の問題>
しかし、それだけではありません。商品名ラゲブリオカプセルは他にも大変な問題を持っています。それは催奇性です。
この「薬」は妊娠前に飲むと赤ちゃんに奇形が発生する可能性が高いことが動物のラットによる実験で分かっています。FDAの「外部有識者会議」でこれと効果の低さに対する懸念が多くでて、賛否わずかの差で緊急使用許可が押し切られたとのことです。
例会では、その他に適正使用量を800mgとした点にも疑問を出しましたが、今回は省きます。
<ワクチン接種者での効果は確かでない>
臨床試験Ⅱa相、Ⅱ/Ⅲ相試験のパートⅡ相もパートⅢ相も「除外基準」に「コロナワクチン接種者」をあげています。この除外基準はワクチン非接種者は「コロナにかかり易く」患者の比率が高くなることが目的化とは思われます。ワクチンの効果はともかく、既にコロナワクチンを接種している人ではどの程度効果があるかを正確に調べられていないことは確かです。
こんなことがあってか、フランスはこの薬の購入契約を、キャンセルし、FDAが同時に「緊急承認」したファイザー製の「飲み薬」に代えると言っています。
効果も不確かで、催奇性があると聞くと、安部前首相のお友達が会長の「富士フィル」子会社が作った抗インフルエンザの「ファビビラビル」も、強引に認可させたものの、その催奇性のためにほぼ使用されていません。インフルエンザではできなかった薬剤認可の無茶が、コロナでは可能、しかも世界的に可能な、危険な状態になっているように思われます。
はやし小児科 林
報告2,ワクチンの有害事象報告は極めて少―ランダム化比較試験(RCT)での報告率との比較―
次の報告は、日本で実際行われたワクチンに関する有害事象報告が極めて少ない点について、RCTでのその報告と比較し、評価しました。
本誌の前号では、Thomasらのランダム化比較試験(RCT)でのワクチン接種者と非接種者の接種後の全死亡(全ての原因による:以下同じ)率が同じ程度であったことを報告しました。例えワクチンが新型コロナ感染による死亡を減らしたとしても、その分有害作用により死亡する人が増えることを意味しています。
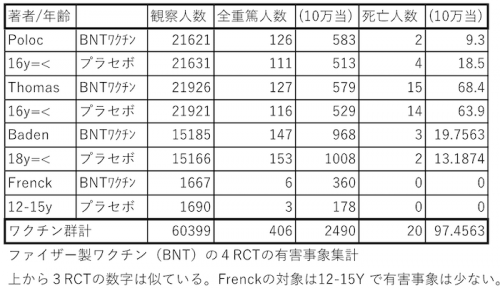
ファイザーワクチンに関してその他のRCTを調べましたが、全死亡者はワクチンとプラセボの両群とも少数で、ほぼ同じでした。(次表)、また(全ての原因による)「全重篤」な有害事象の比率も両群でほとんど同じでした。
大変よく管理されたRCTで調べられた有害事象は他の調査方法よりは、短期かつ比較的多いものに限定すればはるかに正確です。
実際のワクチン接種後の有害事象の追跡は大変いい加減にされていることが予想されます。その一つの証拠は、接種数に対する死亡報告の率は、接種が始まって以後、時間が経るほど極端に減少するという事実です(本誌2021年7月551号と<文献>の下の<参考資料>)。
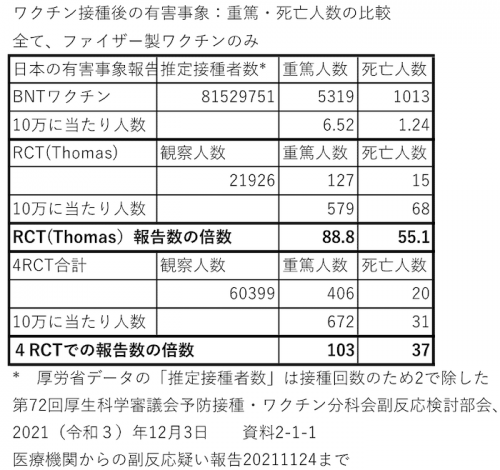
そこで、日本では実際にどれほど正確に報告されているかを、RCTの有害事象のデータと比較して、調べてみました。なお、昨年11月12日までの医療機関からの厚労省への報告の「推定接種者数(回分)は163,059,502回で、一人2回接種しているので、接種人数はこの半分81,529,751人としました。
結果は、下表のように、日本の医療機関からの全報告数は10万人当たり、重篤人数は6.52人、死亡人数は1.24人です。ThomasらのRCTは、10万人当たりそれぞれ579人と68人です。医療機関からの報告と比べ、重篤はこのRCTが実に88.9倍と55.1倍の報告でした。同様に4つのRCT合計では、10万人当たり重篤は672人、死亡は31人で、医療機関からの報告の、重篤は103倍、死亡が37倍でした。
もちろん、日本の医療機関が報告した有害事象は「副作用疑い」として報告されていますので、全有害事象より選別されているものです。しかし、医療機関が、ワクチンと「関連有り」としているのはその1割です。報告者は、より広い範囲の健康障害(有害事象)を報告していると考えられます。にもかかわらず、RCTと比べると、重篤は約100分の1、死亡は数十分の1のみが報告されていることになります。
しかも政府は、その医療機関が「関連有り」とした死亡報告は、1013人のうちの85人ですから、報告者の多くは関連なしと思っても報告しているのです。しかも、厚労省はこれらの死亡者のうち誰一人もワクチンの害作用として認定していません。
このワクチンは昨5月に例外的な「特例承認」されたものであり、有害事象は、疑いかどうかにかかわらず全てを報告すべきでしたが、それが極端に抑えられ、かつ政府によって無視されているのです。
はやし小児科 林敬次
<文献>
Polack FP et al. N Engl J Med 2020;383:2603-15.DOI: 10.1056/NEJMoa2034577
Thomas SJ et al. N Engl J Med 2021;385:1761-73.DOI: 10.1056/NEJMoa2110345
Badem LR et al. N Engl J Med 2021;384:403-16. DOI: 10.1056/NEJMoa2035389
Frenck RW et al. DOI: 10.1056/NEJMoa2107456
<参考資料>
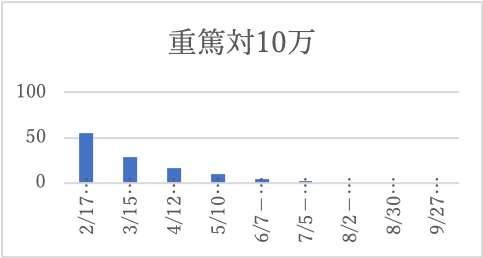
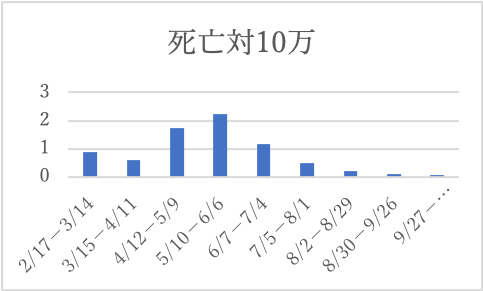
以下の図は、日本でのコロナワクチン接種後の「副反の報告」の医療機関からの報告の、接種回数10万回当たりの推移です。
2021年2月から医療従事者、4月12日から高齢者、一般と経過しています。
「重篤」は激減し続けています。他方で、「死亡」は4月12日の高齢者の開始後著しく増加するも、その後医療従事者よりも激減しています。